随着全球医疗器械市场的不断扩展,俄罗斯作为重要的新兴市场之一,其医疗器械与体外诊断(IVD)产品的注册程序备受关注。数字化工具如小程序的研发,为相关企业提供了高效的管理与查询手段。本文将系统介绍俄罗斯现行的医疗器械与IVD产品注册流程,并探讨小程序在其中的研发应用。
一、俄罗斯医疗器械与IVD产品注册现行程序
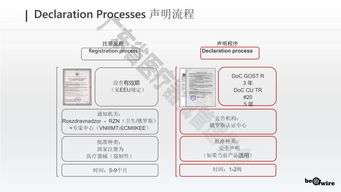
俄罗斯的医疗器械和IVD产品注册由联邦卫生监督局(Roszdravnadzor)负责监管,主要依据《医疗器械流通法》及欧亚经济联盟(EAEU)的相关法规。现行注册程序可分为以下几个关键步骤:
- 准备阶段:
- 确定产品分类:俄罗斯将医疗器械分为I类(低风险)至III类(高风险),IVD产品同样按风险分级。
- 收集技术文件:包括产品说明书、技术规格、质量管理体系证书(如ISO 13485)、临床评估报告等。
- 选择授权代表:非俄罗斯企业需指定当地授权代表,负责与监管机构沟通。
- 测试与评估阶段:
- 进行技术测试:在俄罗斯认可的实验室进行性能、安全性和有效性测试。
- 临床评估:高风险产品需提供临床试验数据,部分低风险产品可豁免。
- 质量管理体系审核:确保符合EAEU或俄罗斯国家标准。
- 提交注册申请:
- 通过Roszdravnadzor的在线系统提交申请,包括所有技术文件和测试报告。
- 支付相关费用,费用根据产品类别和复杂性而定。
- 审核与批准阶段:
- 监管机构审核文件,可能要求补充信息或现场检查。
- 审核通过后,颁发注册证书,有效期通常为5-10年,需定期更新。
- 产品上市后需进行持续监管,包括不良事件报告。
- 特别注意事项:
- 自2022年起,俄罗斯逐步推行EAEU统一注册制度,旨在简化跨国流程,但过渡期内仍可能存在国家特定要求。
- 地缘政治因素可能影响注册时间,建议企业密切关注政策变化。
二、小程序在注册流程中的研发应用
为提升注册效率和管理便利性,研发针对俄罗斯市场的小程序成为新兴趋势。小程序可基于微信、支付宝或俄罗斯本土平台(如Yandex)开发,具有轻量化、易操作的特点。
- 功能设计:
- 法规查询模块:整合俄罗斯及EAEU最新法规,提供实时更新和关键词搜索。
- 流程指导工具:通过交互式界面引导用户逐步完成注册步骤,并生成个性化清单。
- 文件管理:支持技术文件的上传、存储与分类,确保符合格式要求。
- 进度跟踪:连接Roszdravnadzor系统,实时显示申请状态和审核反馈。
- 提醒服务:设置关键节点提醒,如证书续期、测试截止日期等。
- 研发要点:
- 本地化适配:需兼容俄语界面,并考虑俄罗斯用户的网络习惯(如偏好Yandex服务)。
- 数据安全:确保符合俄罗斯数据保护法规(如《个人数据法》),采用加密传输和存储。
- 集成能力:可与企业的ERP或质量管理软件对接,实现数据同步。
- 成本控制:采用模块化开发,根据企业需求灵活定制功能,降低研发成本。
- 应用案例:
- 某中国医疗器械企业通过小程序简化了文件提交流程,注册时间缩短约20%。
- IVD产品供应商利用小程序的提醒功能,避免了证书过期导致的合规风险。
三、挑战与展望
尽管小程序为注册流程带来便利,但企业仍需面对俄罗斯法规的多变性和语言壁垒。随着人工智能技术的融入,小程序或能提供更智能的合规建议,例如自动分析法规变化对产品的影响。加强与俄罗斯本地服务商的合作,将有助于优化用户体验。
理解俄罗斯医疗器械与IVD产品注册程序是进入该市场的关键,而小程序的研发应用则为这一过程注入了数字化动力。企业应结合自身需求,善用技术工具以提升合规效率,从而在竞争激烈的全球市场中占据先机。